식품의약품안전처는 동일한 생동물학적 동등성 시험자료를 이용한 허가 품목 개수 제한(1+3) 내용이 포함된 약사법 개정안을 20일 공포했다.
기존에는 동일한 생물학적 동등성 시험자료를 이용해 추가로 품목허가를 신청할 수 있는 개수 제한이 없어 품목 난립에 따른 과당 경쟁과 제품 품질 저하로 이어졌으나, 추가 품목허가 신청 개수를 3개로 제한해 제약산업의 경쟁력을 강화한다.
7월 20일까지 다수의 의약품 제조업자가 공동개발하기로 하고 임상시험계획 승인을 받은 의약품의 경우, 품목 수 제한 적용을 받지 않으려면 올해 8월 19일까지 관련 계약서와 관련 증빙자료 등을 첨부해 의약품 공동개발 사실을 신고해야 한다.
식약처가 공개 제시한 '동일 임상(생동)시험자료를 이용한 품목 수 제한 관련 Q&A' 자료에 따르면, "본 개정 규정 1+3 시행 전에 특정 임상(생동)시험자료를 사용하도록 여러 번 동의한 경우 더이상 해당 자료를 이용해 품목허가 등을 받을 수 없는지?"에 대해 식약처는 "본 개정규정 1+3 시행 전에 특정 임상(생동)시험자료를 사용하도록 여러 번 동의한 경우라도 부칙 제11조에 따라 본 개정규정 1+3 시행 후부터 3회에 한해 해당 임상(생동)시험자료를 사용할 수 있도록 추가 동의가 가능하다"고 밝혔다.<그림1 참조>
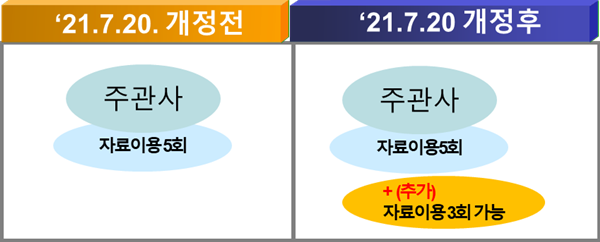
또한, "공고 대조약 고함량 품목과 ①생물학적 동등성을 입증한 고함량 품목 및 ②비교용출시험자료를 제출해 허가받은 저함량 품목의 경우 각 함량별로 3회씩 생물학적 동등성시험자료 사용의 동의가 가능한지?"에 대해 식약처는 "②저함량 품목의 경우, ①고함량 품목의 생물학적 동등성을 기반으로 허가받은 것이기 때문에 저함량, 고함량 품목은 묶음으로 자료사용이 동의됐다고 볼 수 있다. 저함량 품목이든 고함량 품목이든 3회의 생물학적 동등성시험자료 사용의 동의가 있으면 추가로 자료사용 동의가 가능하지 않다"고 설명했다.<그림2 참조>
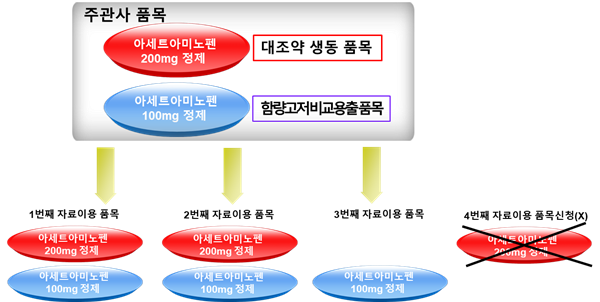
공동개발과 관련해 "본 개정 규정 1+3 시행 전부터 공동개발 중이었으나 시행 당시에 임상시험계획 승인을 받지 못한 의약품의 개발자도 공동개발 사실을 신고해 본 개정 규정 1+3의 적용을 받지 않을 수 있는지?"에 대해 식약처는 "부칙 제10조에 따르면, 본 개정 규정 1+3 시행 전부터 공동개발 중이었다고 해도 본 개정 규정 1+3 시행 당시에 임상시험계획이 승인되지 않은 경우에는 본 개정 규정의 적용을 받게 된다"고 했다.
이와 함께, "본 개정규정 1+3 시행 전 공동개발하기로 하고 임상시험계획을 승인받은 경우, '의약품 위탁제조판매업자'도 공동개발 사실을 신고해 본 개정 규정 1+3의 적용을 받지 않을 수 있는지?"에 대해 "부칙 제10조에 따르면, 본 개정 규정 1+3 시행 전 공동개발하기로 하고 임상시험계획을 승인받은 의약품에 대해서는 공동개발하기로 한 ‘의약품 제조업자’에 한해 해당 규정을 적용받지 않도록 규정하고 있으나, 해당 규정의 취지상 의약품 제조업자 외에 '위탁제조판매업자'도 이에 포함해 해석할 수 있을 것으로 판단된다"고 밝혔다.
또한, "본 개정규정 1+3 시행 전 공동개발하기로 하고 임상시험계획을 승인 받은 의약품에 대해 공동개발 사실을 신고하려는 경우 제출해야 하는 자료는?"에 대해 식약처는 "본 개정규정 1+3 시행 당시 의약품을 공동개발하기로 하고 임상시험계획 승인을 받은 자가 해당 사실을 신고하려는 경우, 공동개발 사실이 명확히 기재된 계약서 등을 공증받아 제출해야 한다. 이 경우 공동개발 계약서에는 공동개발하려는 제품을 특정할 수 있는 정보 및 공동개발 추진 시 업무 또는 비용의 분담에 관한 사항이 포함돼야 하며, 계약서상의 공동개발자 정보는 이후에 품목허가를 신청하는 의약품의 제조업자 정보와 동일해야 한다"고 했다.
우정헌 기자 medi@mediherald.com
<저작권자 © 메디컬헤럴드, 무단 전재 및 재배포 금지>

