식품의약품안전처(처장 김강립)는 의약품 유통 안전·관리 기준을 강화하고 의약품 허가·심사 제도운영 기준을 개선하는 것을 주요 내용으로 하는 '의약품 등의 안전에 관한 규칙'(총리령)을 1월 20일 개정·공포했다고 밝혔다.
◆'의약품 유통 안전·관리 기준' 강화= 의약품 품목허가를 받은 자, 수입자, 의약품 도매상은 냉장·냉동 보관이 필요한 의약품(생물학적 제제등 포함) 운송 시 자동온도기록장치를 갖추고 의약품의 운송기록에 온도를 포함하도록 한다.
아울러, 의약품 품목허가를 받은 자, 수입자가 이를 위반한 경우에 대한 행정처분 기준도 마련했다. (시행: 생물학적제제 등 ’22.1.20, 냉장·냉동 의약품 ’22.7.21.)
위반시행정처분은 (1차) 해당품목 판매업무 정지 3개월→(2차) 6개월→(3차) 허가 취소 등이다.
의약품 공급자가 전산으로 의약품 공급내역을 보고(마약류의 경우 마약류통합관리시스템)하면 의약품 입·출고에 관해 별도로 기록·보관하지 않아도 되도록 개선한다. (시행: ’22.1.20.)
의약품 도매상의 교육의무 대상을 모든 도매상으로 확대하고, 의약품 도매상이 종사자에게 실시해야 하는 자체교육을 한국의약품유통협회에 의뢰해 실시할 수 있도록 한다. (시행: ’23.1.1.)
현행 교육의무 대상은 의약품 유통관리기준(KGSP) 적격업소 도매상 종사자이다.
◆'의약품 등 허가·심사 제도 운영기준' 개선= 완제의약품의 허가를 신청하는 경우 사전에 원료의약품 등록 시 제출한 자료는 제출 면제하고, 원료의약품 등록 시 제출된 자료 이외의 자료는 제출하도록 한다. (시행: ’22.1.20.)
우선심사 대상 의약품은 ‘중증·희귀질환 치료제 중 대체 가능한 의약품이 없거나 안전성·유효성이 현저히 개선된 의약품’으로 명시하고, 특별한 사정이 없으면 90일 이내에 심사한다. (시행: ’22.1.21.)
의약외품 분야에 제조·품질관리기준(GMP)을 도입(권장)해 이를 준수하는 경우 ‘적합판정서’를 발급하도록 한다. (시행: ’22.1.20.)
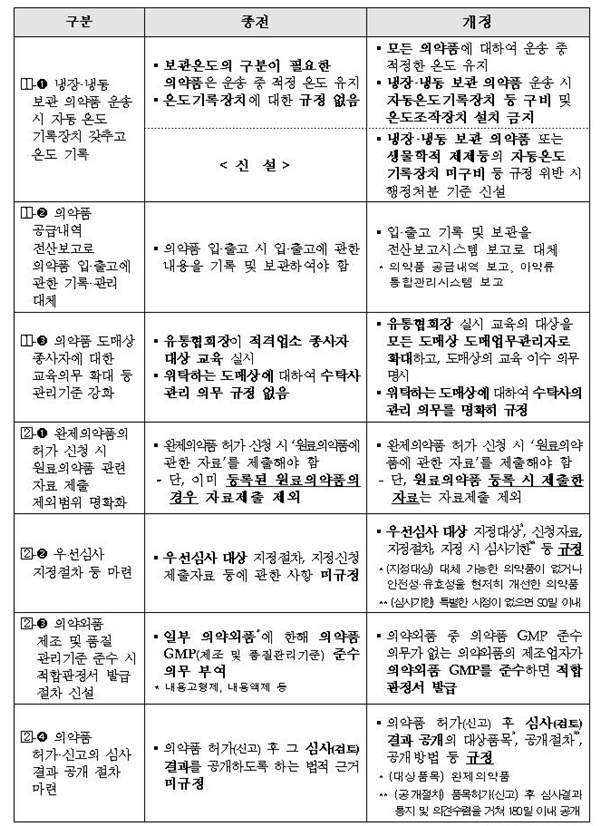
완제의약품 품목허가 이후 허가를 받은 자의 의견을 들어 허가일로부터 180일 이내에 해당 허가심사·검토 결과를 공개한다. (시행: ’22.1.21.)
식약처는 "이번 개정이 의약품 유통 안전·관리 수준을 높이고 의약품 허가·심사 제도를 합리적이고 투명하게 운영하는 데 도움이 될 것으로 기대하며, 앞으로도 과학적 지식과 규제 전문성을 바탕으로 의약품 안전관리 제도를 적극적으로 정비할 계획"이라고 밝혔다.
우정헌 기자 medi@mediherald.com
<저작권자 © 메디컬헤럴드, 무단 전재 및 재배포 금지>

