식품의약품안전처(처장 오유경)는 의료제품 허가심사에 대한 투명성과 신뢰성을 강화하기 위해 12월 5주(12.26.~12.31.) 기간 의료제품 허가 현황을 제공한다고 밝혔다.
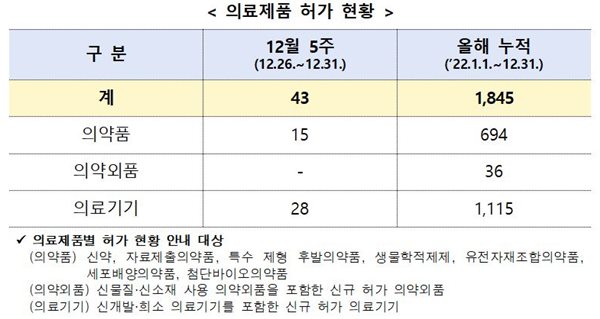
식약처(본부)는 12월 5주(12.26.~12.31.)에 의료제품 총 43개 품목을 허가했다. (2022년 누적: 총 1,845개 품목)
12월 5주에 기존 항바이러스제(간시클로버, 발간시클로버, 포스카네트, 시도포비어)에 내성(또는 불응성)인 거대세포바이러스 감염 환자를 치료하는 희귀의약품인 ‘리브텐시티정200mg(마리바비르)’(한국다케다제약, ’22.12.22.)이 허가됐다.
| * 거대세포바이러스(CMV, Cytomegalovirus): 일반적으로 체내에 잠복해 무증상으로 존재하지만 장기이식 후 면역억제제를 복용하는 환자들에게서 면역억제기간 동안 재활성화되어 심각한 질환 유발 |
식약처 ‘12월 5주 의료제품 허가 품목 리스트 의약품’ 현황에 따르면, ▲리브텐시티정200밀리그램(마리바비르)(한국다케다제약), ▲피마디핀정30/2.5밀리그램(피마사르탄칼륨, 에스암로디핀)(신풍제약), ▲울토미리스주100mg/mL(라불리주맙)(한독), ▲아모노신-에이주(아데노신트리포스페이트이나트륨삼수화물)(휴온스) 등이 포함됐다.
식약처는 “앞으로도 의료제품 허가 현황을 정례적으로 매주 제공하겠으며, 의료제품별 상세한 허가사항은 전자민원시스템에서 확인할 수 있다”고 밝혔다.
우정헌 기자 medi@mediherald.com
<저작권자 © 메디컬헤럴드, 무단 전재 및 재배포 금지>

